媒体报道
近年来,CAR-T细胞疗法在血液瘤领域大放光彩,表现出惊人的效果,但在实体瘤治疗中却举步维艰。与此同时,T细胞受体基因改造T细胞(TCR-T)疗法在部分实体瘤中展现出良好效果,成为一种在癌症治疗中极有潜力的细胞免疫疗法。
随着国内患者增多,TCR-T疗法需求迅速增长。根据中国TCR-T疗法的潜在需求预测,2021至2025年中国TCR-T疗法行业市场规模从387.0亿元增长至1041.4亿元,年复合增长率达到28.1%。
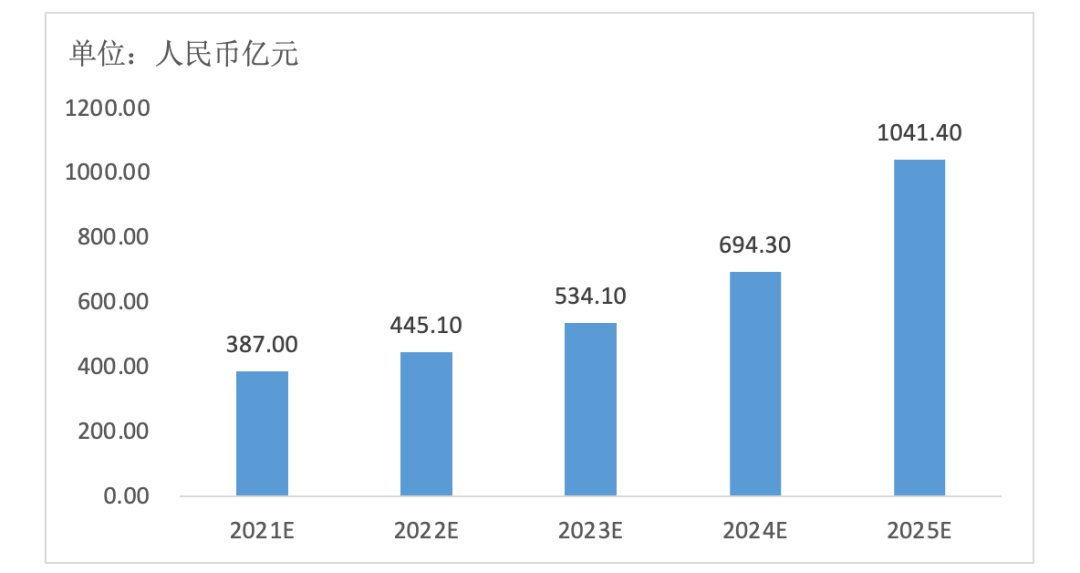
中国TCR-T疗法市场规模预测
T细胞杀伤肿瘤细胞的作用机制
TCR-T技术,即细胞受体(TCR)嵌合型T细胞技术,也叫亲和力增强“TCR”技术。它的目的是让自身的杀手T细胞识别能力更强,因为原本的T细胞对肿瘤相关抗原的识别能力较弱,现在通过基因修改的方式增强识别亲和性,从而使T细胞攻击肿瘤细胞,达到治疗肿瘤的效果。其中抗原提呈是其中关键环节。几乎所有细胞表面都表达HLA-I型分子(人类白细胞抗原),当肿瘤细胞某些蛋白发生突变,就会被蛋白酶切割成小片段的肽段,然后在内质网被HLA-I结合,形成多肽-HLA复合物(pHLA),并运至细胞表面。活化的细胞毒性T细胞(CTL)一旦确定该细胞发生变异就会对其进行破坏,由此达到杀伤肿瘤细胞的作用。
T细胞要完全活化成为功能强大的CTL,需要两种活化信号的协同作用。第一信号为抗原刺激信号,T细胞通过其表面的TCR特异性识别细胞表面提呈着内源肽的pHLA。如此不够,T细胞必须接受第二共刺激信号,只有某些特定的细胞可以同时具备“提供HLA分子展示”和“提供共刺激信号的能力”,这些细胞被称为抗原提呈细胞(APC)。如此,由APC表面的共刺激因子与T细胞表面的相应共刺激分子相互作用产生,使T细胞完全活化。
TCR-T疗法需要从患者身上获取T细胞进行改造,让T细胞表达能够有效识别肿瘤细胞的TCR,使其能够靶向特定的癌症抗原的疗法。这种新型的疗法可以允许医生为每个患者的肿瘤和不同类型的T细胞选择最合适的靶点进行工程改造,使治疗个体化。
与靶向癌细胞表面蛋白的嵌合抗原受体(CAR)修饰的T细胞不同,TCR-T细胞疗法能够通过识别与细胞表面免疫相关蛋白结合的蛋白片段,靶向通常在细胞内发现的蛋白。而找到理想的靶抗原是这一技术起效的关键。
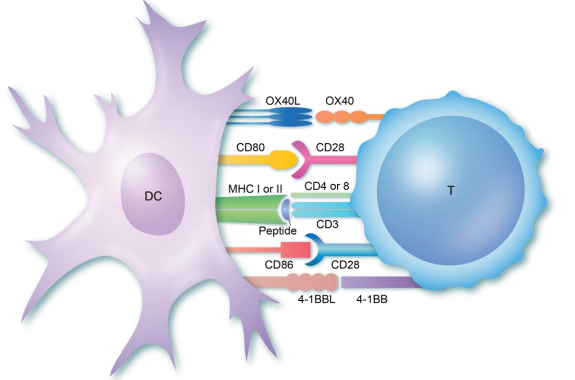
T细胞活化示意图
完全活化的T细胞在多种细胞因子(IL2、IL6、IL12、INF-γ等)的作用下增殖、分化、依赖或不依赖Th(由CD4 T细胞分化得到的辅助T细胞),初始CD8 T细胞分化为细胞毒性T细胞(CTL)。CTL可通过释放穿孔素和颗粒酶等诱导肿瘤细胞凋亡。除了在CTL激活中起辅助作用外,Th可以通过释放细胞因子激活巨噬细胞等杀伤肿瘤细胞。
TCR-T疗法技术介绍
TCR疗法中主要包括TCR蛋白药物和TCR-T细胞疗法。
TCR蛋白药技术:TCR蛋白药是一种新型双特异性T细胞衔接器,由工程化改造的TCR和抗CD3的scFV组成,改造后的TCR具备更高的亲和力(通常为pM级别),可高效地特异性识别并结合肿瘤细胞表面pHLA,抗CD3的scFv通过与CD3相互作用招募T细胞至肿瘤细胞周围,并激活T细胞发挥杀伤作用。
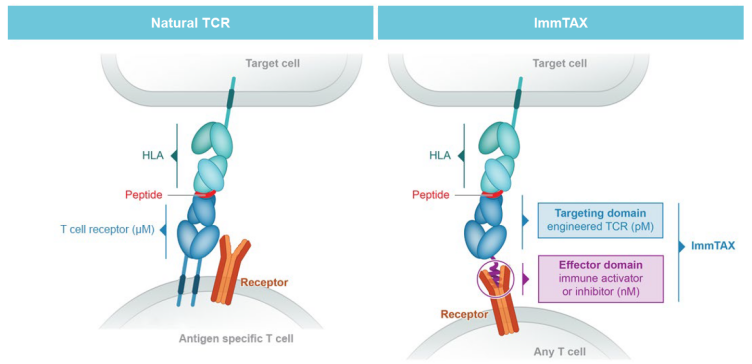
TCR蛋白药物作用机制
目前,已经有1款靶向gp100(在黑色素细胞中低表达,黑色素瘤细胞中高表达)的TCR蛋白药物成功获得FDA批准。这款治疗药物是FDA批准的第一个用于治疗不可切除或转移性葡萄膜黑色素瘤的疗法,也是FDA批准的第一个T细胞受体(TCR)治疗药物。
TCR-T细胞治疗技术:TCR-T细胞治疗是将筛选(或进一步亲和力优化)得到的能够特异性识别并结合pHLA的TCR,通过转基因的方式整合到患者自体T细胞中,使其能够被T细胞高表达,并将这些表达了TCR的T细胞(TCR-T)体外培养扩增之后回输至患者体内,这样当肿瘤表面提呈的pHLA活化了TCR-T后,就能极大地增强了患者对肿瘤组织的靶向杀伤能力。在TCR-T细胞治疗中,多项研究进入临床II期,其中进展最快的靶点主要是MAGR-A、NY-ESO-1、HPV E6/7等。
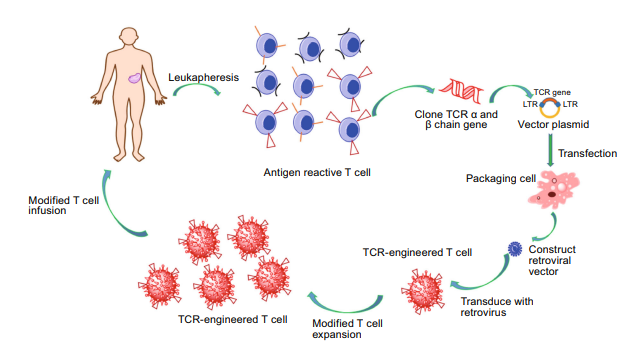
TCR-T细胞治疗流程图
TCR疗法的技术特点:
目前,TCR疗法在TCR在技术中既存在优势又存在一定的局限性,TCR疗法的技术优势主要体现靶点范围广、渗透性好以及副作用少。TCR在局限性方面主要体现在HLA受限,并且仍旧存在免疫逃逸、免疫抑制问题。
与TCR-T细胞疗法对比,TCR蛋白药的成本更低、可及性更好,可推广至更多的适应症和一线治疗。相比TCR蛋白药,TCR-T细胞治疗可诱发表位扩展效应,TCR-T回输治疗后可激活患者体内T细胞对其他肿瘤抗原表位的识别,一定程度上防止肿瘤免疫逃逸。
TCR疗法具有高壁垒:
技术壁垒高:TCR靶点的选择、亲和力和优化都是比较困难的,另外TCR-T对回输数量的要求也更大。
肿瘤易逃逸:TCR-T的活化依赖MHC-I类分子将肿瘤抗原呈递给TCR-T,需要共刺激信号灯,细胞活化过程比CAR-T困难,肿瘤细胞易逃逸其杀伤。
使用人群存在局限:由于人群中MHC的多样性,而TCR-T对肿瘤细胞的靶向杀伤需要MHC分子,因此TCR-T疗法无法像CAR-T疗法一样研发出通用型TCR-T,这点限制了TCR-T的使用。
小结:
目前,尽管TCR-T疗法在临床前或临床前研究中展现出巨大潜力,但依旧存在诸多挑战,相信在未来TCR-T必将展现出独有魅力,给肿瘤患者带来希望。
